이 레포트는 알코올의 증류, 그 중에서 에탄올 증류에 대한 보고서이다.
증류는 끓는점 차이를 이용해 물질을 분류하는 방법의 하나이다.
두 혼합물을 함께 넣고 끓인 뒤 끓는점이 낮은 물질이 먼저 끓어 오르면, 그 증기를 냉각시켜 순수한 물질을 얻어낼 수 있다.
증류에는 단순 증류와 분별증류가 있는데, 분별증류는 연속적인 증발과 응축을 통해 단순증류보다 더 순수한 결과물을 얻을 수 있다. 끓는점이 낮은 물질부터 분리되어 끓는점이 가장 높은 물질은 늦게까지 잔류하게 된다. 원유의 분리에 이용된다.
<실험 과정>
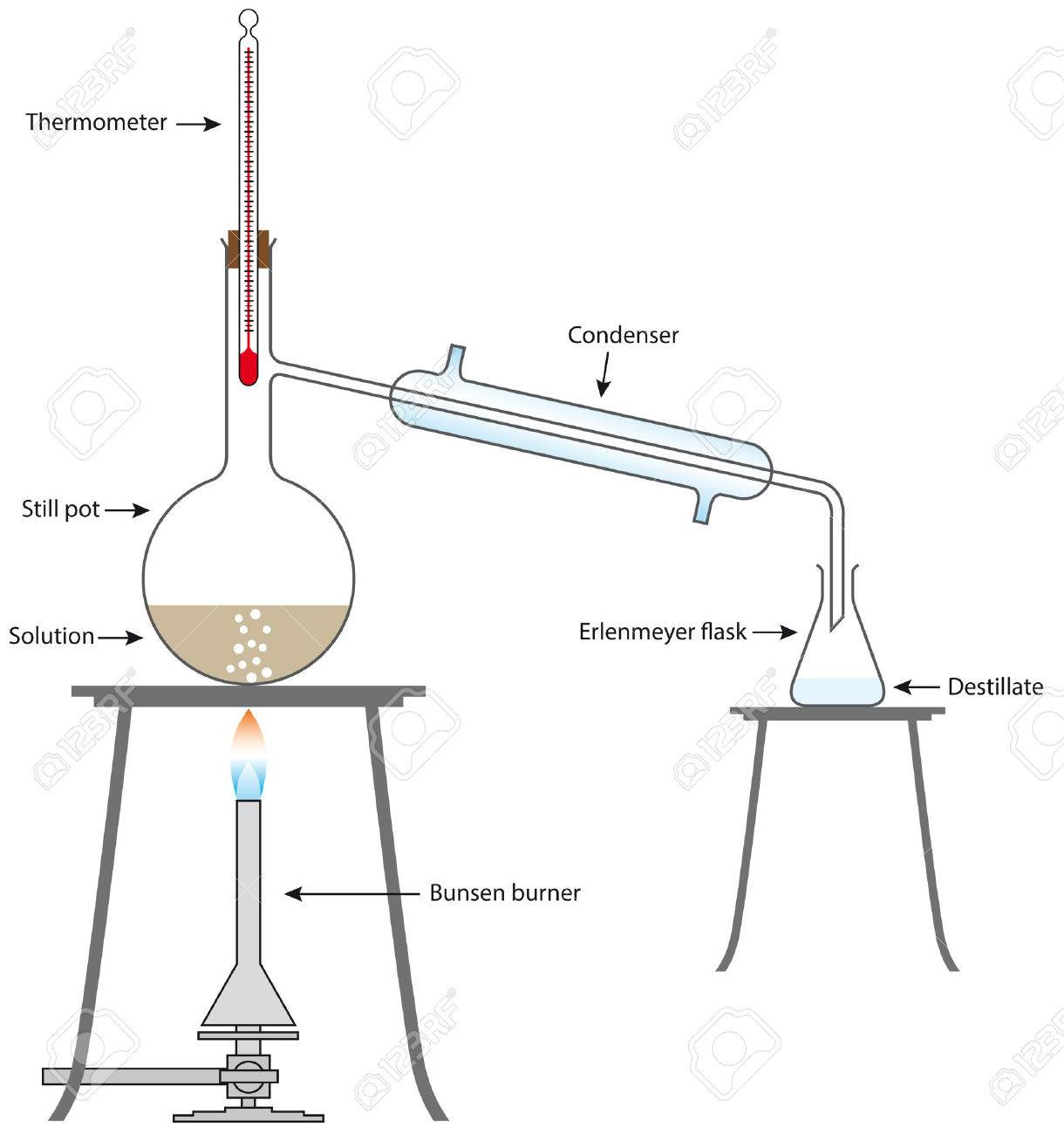
1. 식용색소를 첨가한 에탄올 10.0mL을 둥근바닥 플라스크에 넣고 단순증류장치를 설치한다. (teflon tape로 잘 막는다.)
2. 플라스크를 물중탕하며 가열시킨다. 물의 온도가 50도가 된 순간부터 1분간격으로 온도를 측정하고, 알코올이 분리되어 나오는 것을 확인한다.
3. 온도가 떨어지는 시점부터 3분간 온도를 더 기록한 뒤 실험을 종료한다.
<실험 결과>
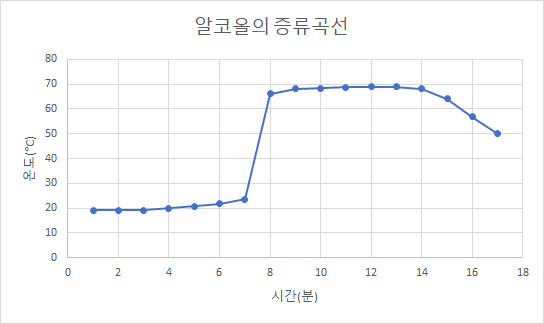
x축을 시간, y축을 온도로 놓고 엑셀로 그래프를 그리면 이러한 그래프가 그려진다.
얻은 알코올의 양 : 17.305-16.334 = 0.971 (g)
수득률 (유효숫자 3자리)
실험실 온도가 21.1도였고, 이에 따른 에탄올 밀도는 0.789 g/mL이므로
0.789 g/mL x 10.0 ml = 7.89g
0.971/7.89=12.3%
<Further Questions>
1)오차의 원인을 서술하시오.
연결부를 막을 때 사용한 teflon tape가 충분히 틈새를 막지 못해 기체가 실험 도중에 밖으로 새어나갔을 가능성이 있다.
2) 증류의 효율을 향상시키기 위해서 개선할 사항 두 가지를 제시하시오.
증류관의 길이가 길수록 순도가 높은 물질을 얻을 수 있기 때문에, 수득률과 효율이 높아진다.
한번 증류된 물질을 재증류하면 순도높은 물질을 얻을 수 있다.
효율이 높은 vigreux 컬럼을 사용한다.
3) 온도가 급격히 증가하는 구간에서 온도가 급격히 증가하는 이유는 무엇인가?
온도계로 측정한 온도는 둥근 플라스크 상단 내부공기의 온도이다. 물중탕으로 증류실험을 진행했기 때무에 물이 데워지는 시간과 열에너지가 에탄올로 전달되는 시간이 필요하다. 물이 충분히 가열되면 에탄올로 전달되는 열에너지가 급격히 증가한다. 이때 알코올이 증발하면서 데워진 알코올 증기가 플라스크 상단의 온도계 쪽으로 올라간다. 따라서 측정된 온도가 급격히 올라간다.
4) 온도가 내려가면 실험이 종료된 것으로 판단할 수 있는 이유는 무엇인가?
끓는점이 물보다 낮은 알코올이 모두 증발하고 냉각되어 증류과정이 끝나면 플라스크 안에는 증발할 알코올이 더이상 남아있지 않게 된다. 따라서 뜨거워진 알콜 증기가 더이상 온도계로 올라와 부딪히지 않기 때문에 측정되는 온도가 낮아진다. 또, 플라스크 바닥의 에탄올은 불순물 (색소)를 포함하고 있어서 순수한 알콜 (위의 증기)보다 끓는점이 높아 끓는 속도가 더 느리다. 실험이 끝나는 시점에는 바닥의 에탄올보다 온도계에 맺힌 에탄올이 기화하는 속도가 더 바르므로 기화열 흡수에 따라 온도계의 온도가 내려가게 된다.
5) 주위 압력이 증가하고 감소할 때의 끓는점의 변화를 설명하시오.
액체는 주변 압력과 증기압력이 같을 때 끓는다. 따라서 외부압력이 높아지면 액체도 더 높은 압력이어야 끓을 수 있기 때문에 액체의 끓는점이 높아진다. 같은 이치로 외부압력이 낮아지면 액체의 끓는점도 낮아지게 된다 주변의 압력이 변화함에 따라 기체가 기화하는 정도가 다르기 때문이다.
6) 감압증류가 무엇인지 설명하고 예를 제시하시오.
감압증류는 낮은 압력에서 물질의 끓는점이 낮아지는 현상을 이용하는 증류방법이다. 일반적인 증류는 액체가 끓을 때까지 가열해 분리하지만 열에 불안정하거나 끓는점이 매우 높은 물질을 분리할 때는 감압증류를 이용해 끓는점을 낮춰 낮은 온도에서도 물질을 증류할 수 있다 대표적으로 석유를 정제할 때 이용되는데, 물질마다 끓는점이 달라 원유에 포함된 여러 성분들을 분리하고 불순물을 제거할 수 있다.
'실험 노트 > 일반화학' 카테고리의 다른 글
| [일반화학실험] 산화-환원 적정: Fe2+와 Ce4+의 반응 (3) | 2024.11.10 |
|---|---|
| [일반화학실험] 휘발성 물질의 몰질량 (3) | 2024.10.10 |
| [일반화학실험] 아스피린 이야기 (아스피린 합성) (0) | 2024.10.07 |
| [일반화학실험] 아보가드로 수의 결정 (0) | 2024.10.03 |
| [일반화학실험] 생활 속의 산-염기 분석 (적정, 역적정 실험) (0) | 2024.10.01 |



